- 联系人 :
- 地址 : 武汉市东湖高新技术开发区光谷七路128号 中科开物产业园枢密脑科学技术有限公司
- 邮编 : 430074
- 所在区域 : 湖北
- 电话 : 181****1572 点击查看
- 传真 : 点击查看
- 邮箱 : marketing@brainvta.com
基因敲入
简介
CRISPR/Cas(Clustered Regularly Interspaced Short Palindromic Repeats/ Cas)系统是目前被广泛运用的基因编辑系统,其原理是由CRISPR转录产生的gRNA介导Cas核酸酶靶向目标序列,对序列进行切割。其中最常用的是靶向DNA的CRISPR/Cas9系统,此系统是由II类CRISPR/Cas系统改造而来,能够在植物、细菌、酵母、鱼类及哺乳动物等多种细胞中,进行有效的靶向编辑,具有操作简易、效率高、以及作用靶位点多等优势。
CRISPR/Cas9系统中sgRNA(short guide RNA)识别并结合目标基因的靶向序列,引导Cas9对结合位点进行剪切,产生DNA双链断裂,通过细胞内的同源重组修复方式,将外源供体DNA定点导入至基因组的靶位点中,从而实现基因敲入。
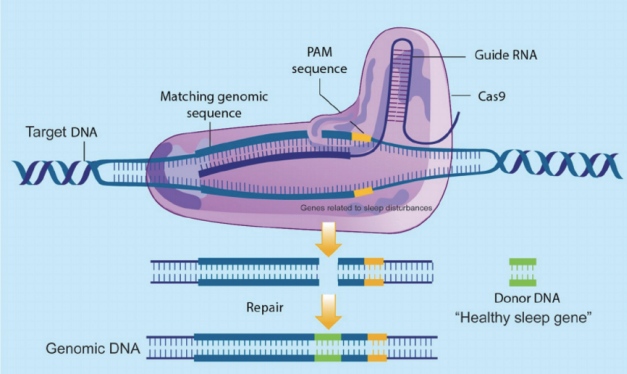
CRISPR/Cas9基因敲入示意图(Eric Murillo-Rodríguez et al., Sleep and Vigilance, 2018)
应用
1.CRISPR/Cas9基因片段敲入细胞系建立
2.CRISPR/Cas9基因单碱基突变细胞系建立
3.CRISPR/Cas9基因敲入建立动物疾病模型
技术优势
1.操作简易:仅需Cas9核酸酶、sgRNA和供体DNA片段(donor),即可定点敲入外源基因片段;
2.效率高:在基因组水平上编辑目标基因,高度模拟目标模型,可精确编辑基因组;
3.广谱性:无物种限制、无细胞种类限制;
4.提供多种基因编辑病毒工具:AAV、LV;
5.提供BSL-1和BSL-2病毒注射及实验操作平台;
6.全面的实验技术支持。
服务内容
1.sgRNA的设计;
2.细胞内sgRNA剪切活性筛选;
3.敲入载体的构建:Cas9-sgRNA表达质粒、donor质粒;
4.依据所要编辑的细胞选择Cas9、sgRNA和donor不同导入方式:
a、脂质体易转染细胞:使用质粒系统( Cas9、sgRNA和donor ) ;
b、脂质体难转染细胞:使用质粒系统电转化、慢病毒或腺相关病毒感染( Cas9、sgRNA和donor ) ;
5.筛选基因敲入单克隆细胞系。
服务流程
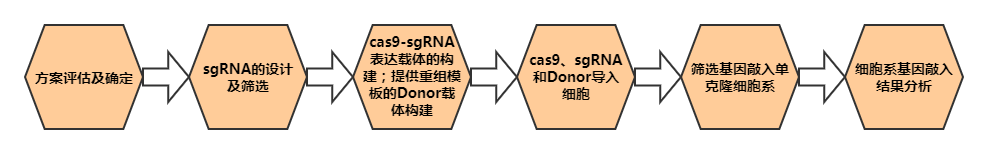
客户提供
1. 目的基因序列(序列/ID)以及物种来源;
2. 靶细胞系及细胞培养条件(可选);
3. 病毒类型选择以及要求;
4. 血清型选择。
服务信息及最终交付内容、产品
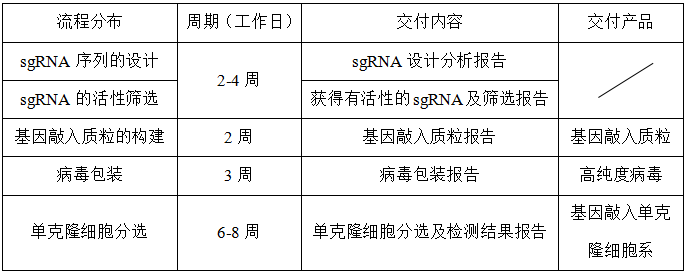
声明:枢密科技提供的所有基因编辑服务及该服务的后续研究,仅适用在国家法律和伦理规范的范围内实施。禁止用于任何人体或临床实验的研究;禁止用于对人类生殖体系进行基因修饰的研究;禁止将基因修饰的其他动物胚胎及生殖细胞植入人体。客户如违反相关法律规定,本公司不承担任何法律责任。
案例展示
Yang H等人研究发现,通过同源重组在Nanog基因第4个外显子末端插入报告基因荧光蛋白cherry(A)。Southern显示重组成功(B)。Nanog基因只在胚胎干细胞表达,干细胞分化后Nanog基因不再表达,表现为干细胞表达荧光蛋白cherry,分化后的细胞无荧光(C)。
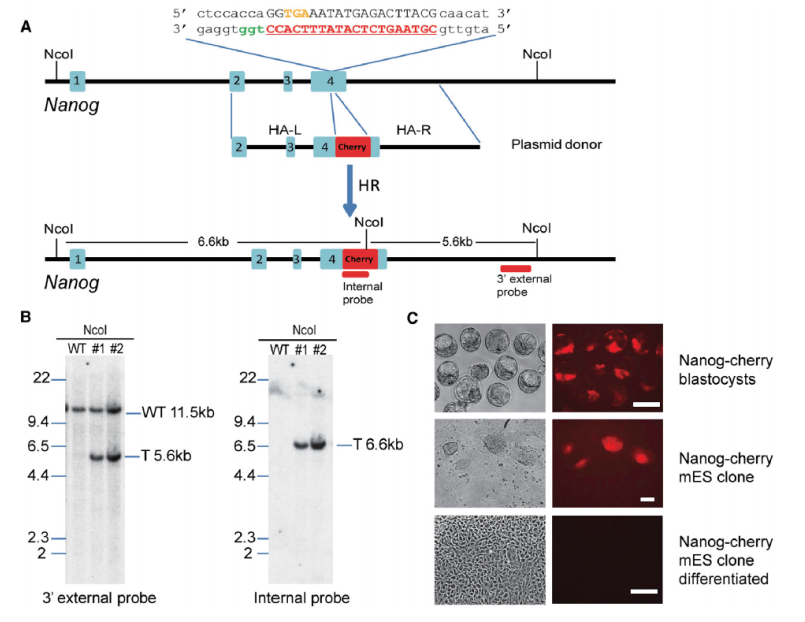
(Yang H et al. Cell, 2013)
参考文献
[1] Eric Murillo-Rodríguez, Rocha N B , André Barciela Veras, et al. The End of Snoring? Application of CRISPR/Cas9 Genome Editing for Sleep Disorders[J]. Sleep and Vigilance, 2018, 2(1):1 3-21.
[2] Yang H, Wang H, Shivalila CS, et al. One-Step Generation of Mice Carrying Reporter and Conditional Alleles by CRISPR/Cas-Mediated Genome Engineering. Cell. 2013;154(6):1370-9.
