
可溶性微针(DMN)作为疫苗输送的新型递送系统,疫苗被整合到微针结构中,在皮肤上使用时,微针穿透角质层,并将疫苗传递给身体,产生免疫反应。爱尔兰科克大学药学院Abina M. Crean教授利用MicroFab的压电喷墨打印技术,在高500μm,底部直径166μm的微针上,成功制备了双层DMN。压电喷墨技术在皮升范围内的液滴体积精度变化为5%,可以精确控制液体制剂的分配,是商业化制造含有临床相关流感疫苗的双层DMN的前沿技术。
介绍
皮肤是一种免疫功能丰富的组织,也是人体最大的器官。理论上,皮肤是疫苗和药物分子传递的理想目标。然而,由于皮肤外层坚硬、富含脂质的角质层,大多数生物药物和小分子都无法渗透皮肤。可溶性微针(DMN)作为疫苗输送的新型递送系统,疫苗被整合到微针结构中,在皮肤上使用时,微针穿透角质层,并将疫苗传递给身体,产生免疫反应。这种经皮疫苗输送系统消除了利器废物和针刺损伤的风险,且与涂层微针装置相比,可溶解的微针拥有更高的药物负载。
DMN的常规生产方法是将液体制剂分配到聚二甲基硅氧烷(PDMS)模具中,然后进行干燥。但是PDMS具有疏水性和高界面张力等特性,故其生产时模具润湿不足会导致空气滞留在其孔内,导致微针尖端形成较差。压电喷墨技术是一种“按需”的喷墨打印技术,允许生产低皮升范围(1-70皮升)的液滴尺寸,配合运动平台可以实现定位精确地分配。科克大学药学院研究的主要目的是利用压电喷墨技术制备双层DMN,除了制造微针结构外,重要的是还要证明在配药过程中保持了要纳入DMN的候选疫苗的完整性。因此,还有部分研究是证明压电分配后的季节性流感疫苗的完整性。
利用MicroFab微液滴发生系统以及Thorlabs步进电极搭建的样品制备平台如图1和图2所示。
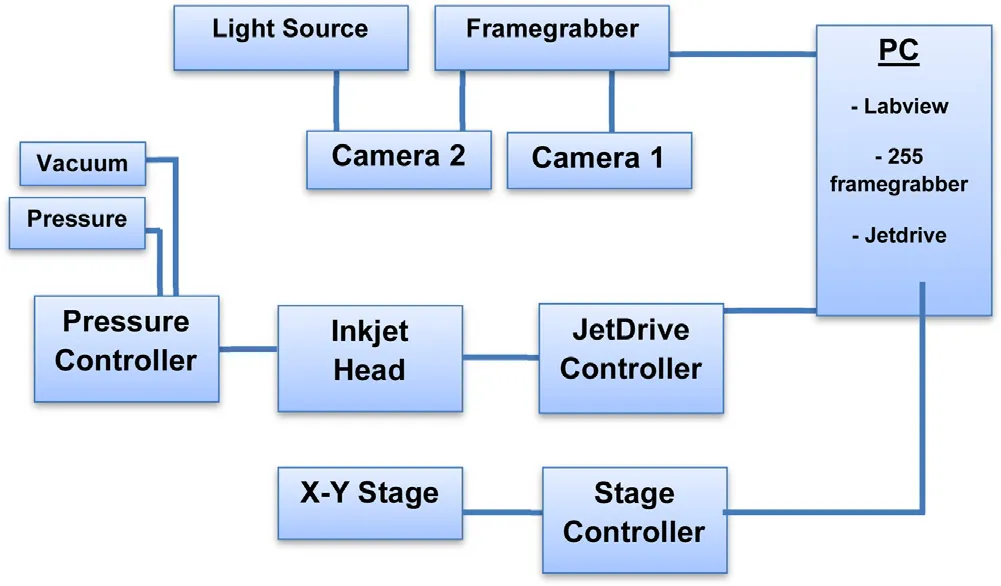
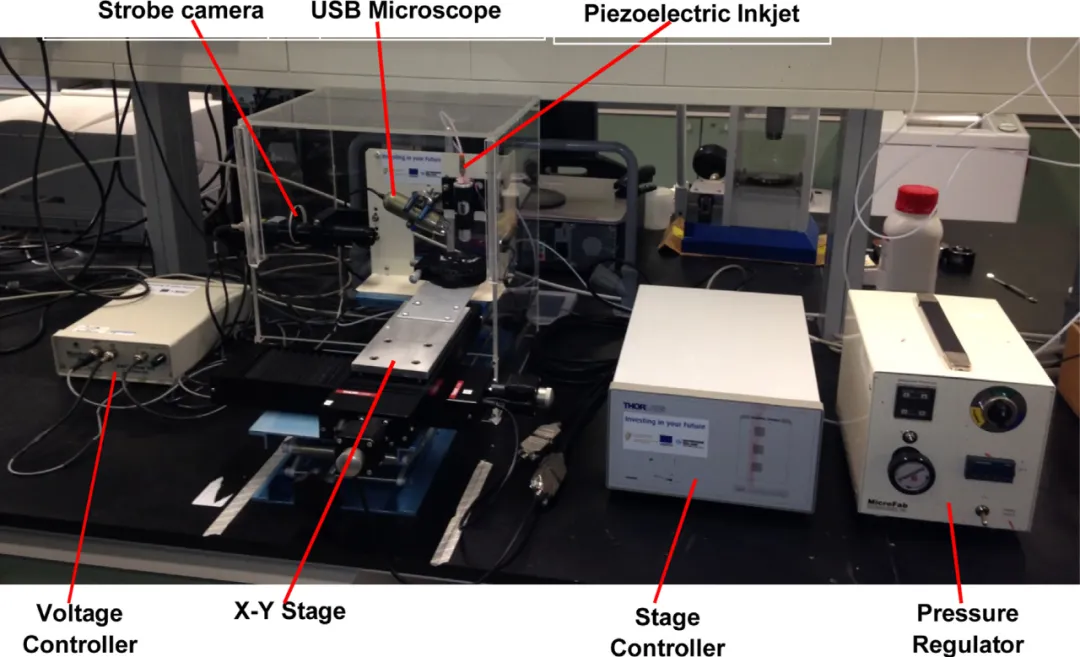
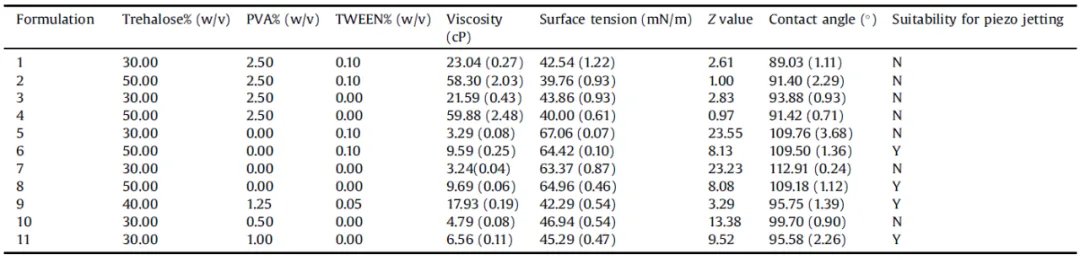
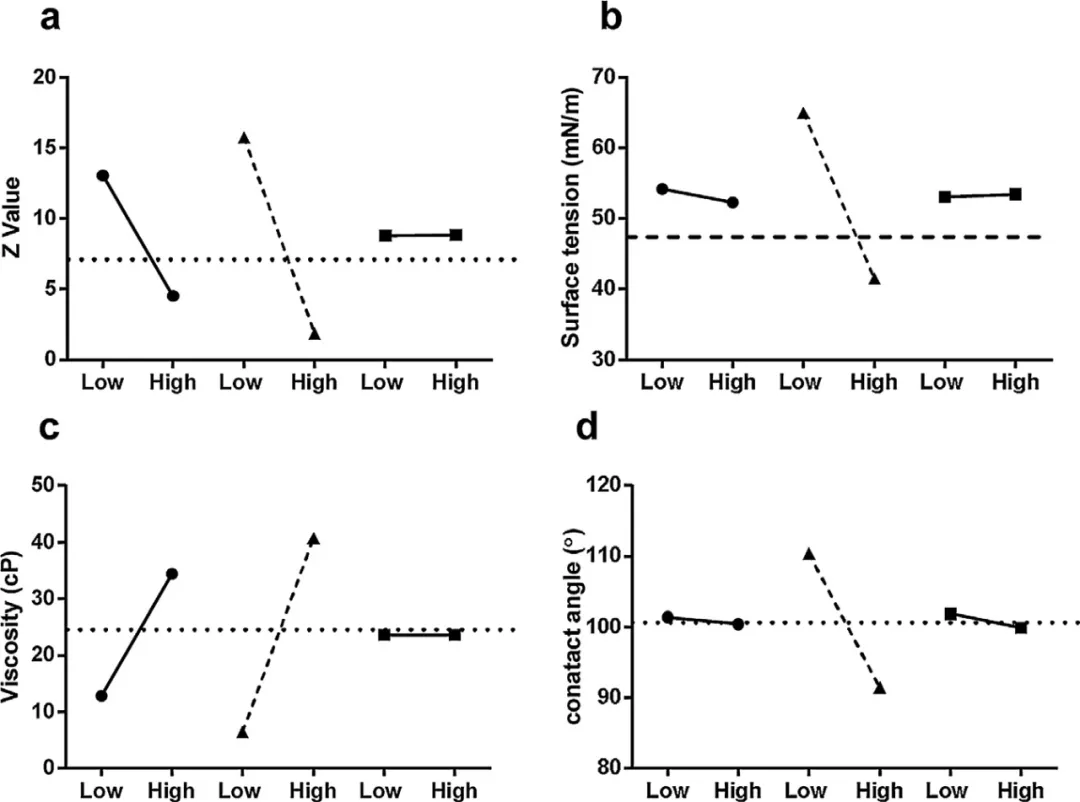
在开发按需液滴分配系统时,可以形成稳定的液滴是精确分配液体制剂到微针孔的关键。采用喷口直径80µm的压电喷头(MicroFab),在压电驱动后50-400µs的时间段内,使用CCD相机的频闪图像捕获捕获的液滴形成图像。两种配方均在30V和50Hz频率下启动。图4(a)30%海藻糖水性制剂形成卫星滴;图4(b)30%海藻糖/1%聚乙烯醇水溶液形成稳定液滴。

| ▲ 图4a | ▲ 图4b |
在压电驱动后50-400µs的时间段内,使用CCD相机的频闪图像捕获技术捕获30%海藻糖溶液配方的液滴形成图像。图5(a)在高背压和80V时下降驱动,以及图5(b)在低背压和60V时下降启动。所有液滴均以50Hz的频率分配。结果表明,压电分配是一种可行的技术,用于分配具有粘度和表面张力值范围的液体制剂配方。

| ▲ 图5a | ▲ 图5b |
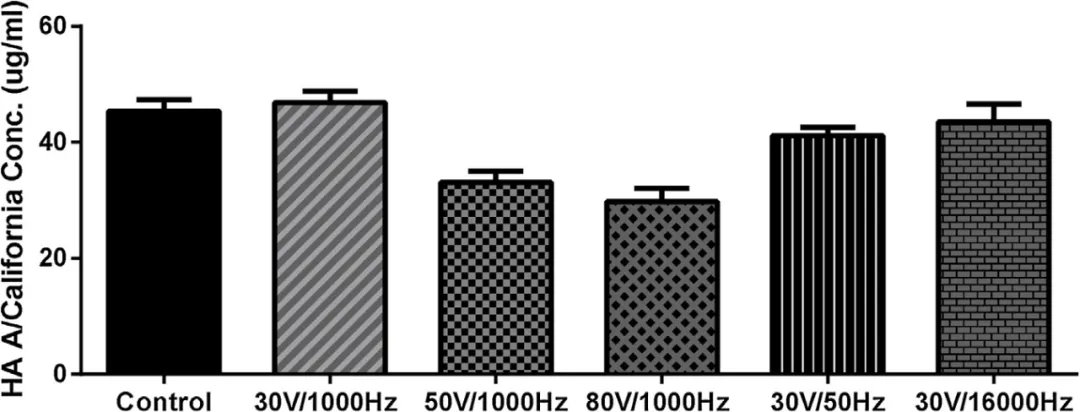
如图6所示,在不同电压(30V、50V和80V)和频率(50、1000和16000Hz)下分配之前和之后,通过SRID分析检查30%(w/v)海藻糖和1%(w/v)聚乙烯醇配方中季节性流感疫苗的生物完整性,结果证明了压电喷墨技术制备三价灭活的亚单位流感疫苗的可行性。


结论
研究结果表明了压电喷墨技术在双层DMN制备中的成功应用,在昂贵的生物溶液或有限的疫苗抗原储备的情况下,这种分配方法是非常可取的,与其他分配技术相比,压电喷墨技术在皮升范围内的液滴体积精度变化为5%,可以精确控制液体制剂的分配,压电喷墨技术已被成功地证明是一种很有前途的、用于商业制造含有临床相关流感疫苗的双层DMN疫苗的技术。
参考文献:
[1] Evin A. Allen et al. Dissolvable microneedle fabrication using piezoelectric dispensing technology[J]. International Journal of Pharmaceutics, 2016, 500(1-2) : 1-10.
