弓形虫被称为世界上最成功的的寄生虫之一,因为几乎所有的恒温动物都能被它感染,包括人类,其中猫科动物是弓形虫感染的唯一终宿主。当然,家养猫咪只要做到定期驱虫、体检和注射疫苗,勿投喂生肉或未煮熟的肉类,避免接触流浪猫,猫砂及时清理、做好防护并及时洗手,减少“吸猫”行为(防止黏膜感染)等,感染的风险就会大大降低了。
口腔包囊感染是弓形虫的主要传播途径,可导致致死性肠道炎症。弓形虫感染改变肠道菌群的组成和代谢,从而影响弓形虫病的进展,然而潜在的机制尚不清楚。2023年12月,云南农业大学李小兵教授/江康峰副教授与团队在Microbiome发表题为“Gut microbiota-related metabolite alpha-linolenic acid mitigates intestinal inflammation induced by oral infection with Toxoplasma gondii”的研究论文,通过建立小鼠模型进行多组学分析,揭示了弓形虫包囊与肠道微生物群之间的相互作用机制,并提示α-亚麻酸(ALA)是治疗弓形虫诱导的肠道炎症的潜在候选药物。(麦特绘谱提供Q200宏代谢组检测服务)

研究思路
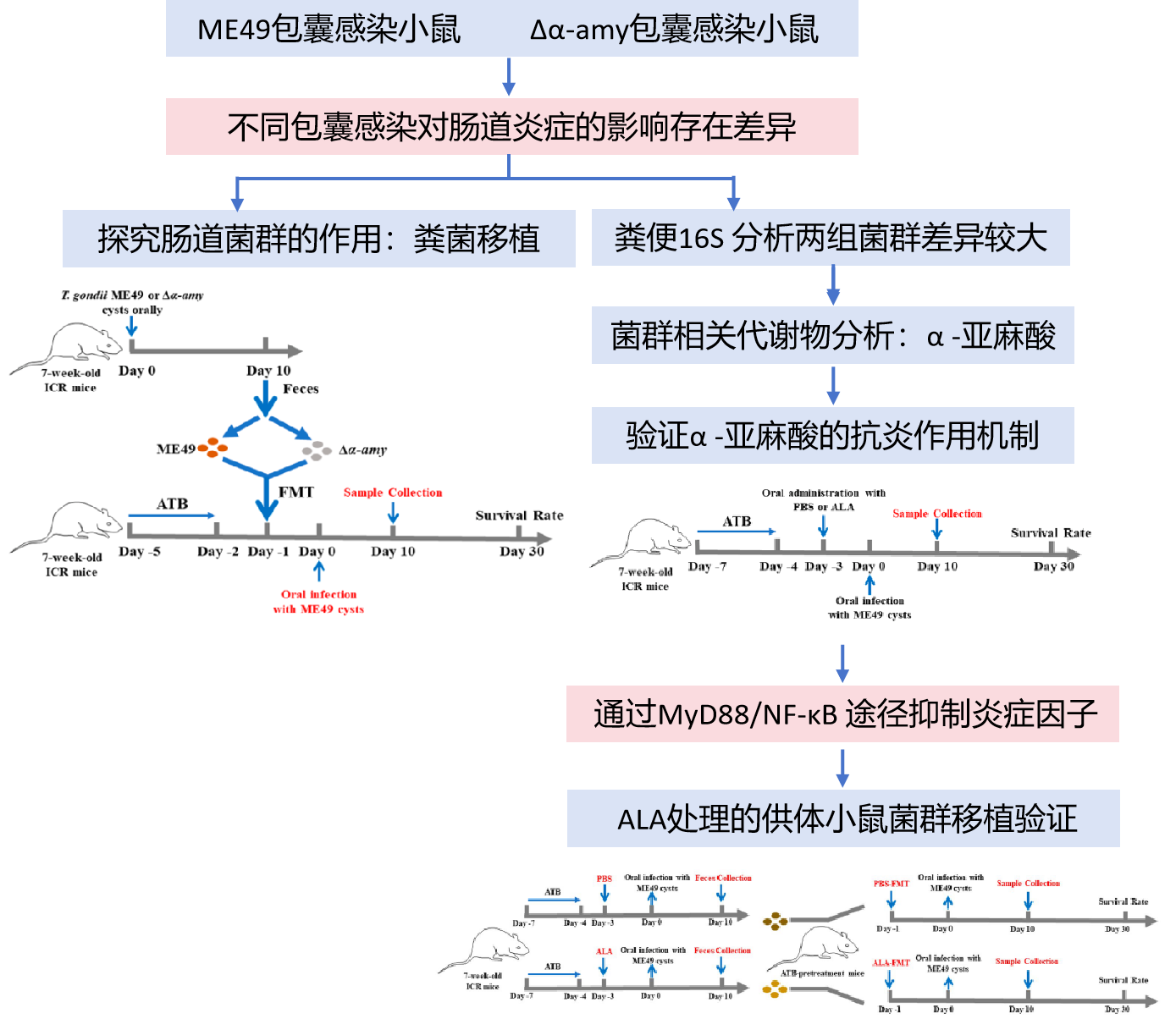
图1. 技术路线
研究结果
1. 通过比较ME49株包囊与Δα-amy包囊对宿主的不同影响,发现Δα-amy包囊对小鼠无致病性,且ME49株包囊和Δα-amy包囊感染的小鼠肠道炎症的严重程度存在显著差异。(弓形虫α-淀粉酶α-AMY是支链淀粉代谢的关键酶,是维持慢性感染的关键,此前研究表明敲除α-AMY后,囊肿功能发生明显改变,可减轻弓形虫病)
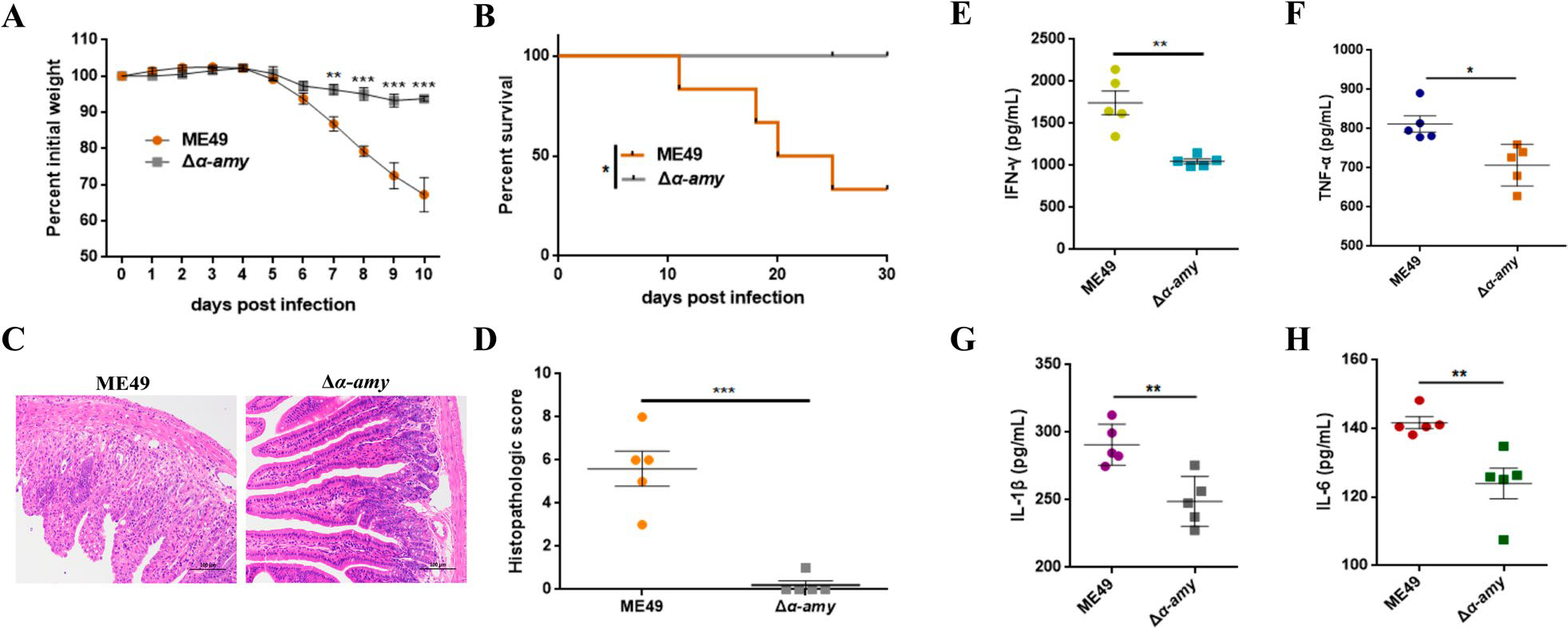
图2. Δα-amy包囊感染可显著缓解弓形虫引起的结肠炎
2. 将不同包囊感染的小鼠粪菌移植给抗生素处理的小鼠体内,发现与ME49-FMT相比,Δα-amy-FMT小鼠能够抵抗弓形虫感染引起的结肠炎,表现为零死亡率,粘膜损伤和炎症细胞浸润明显减轻,炎症因子IFN-γ、TNF-α、IL-1β和IL-6的水平降低。
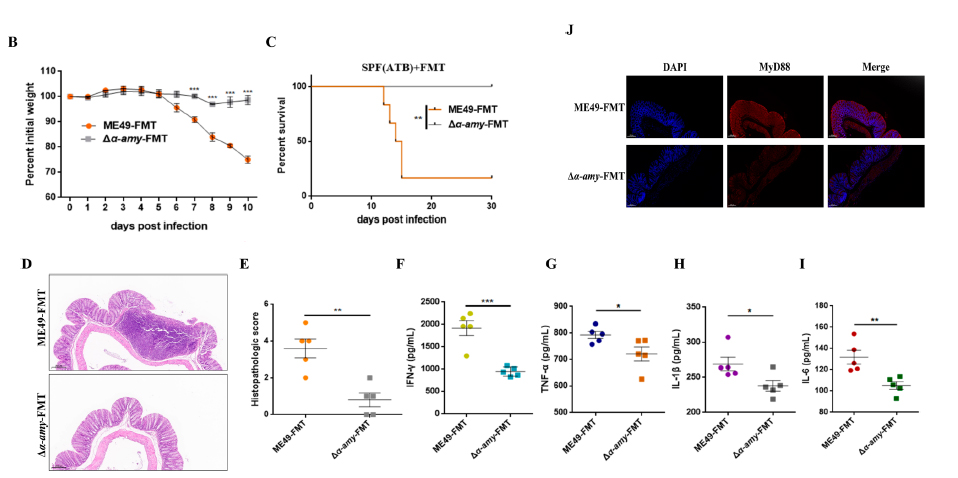
图3. 包囊感染的严重程度与肠道菌群密切相关
3. 粪便16S分析发现,ME49与Δα-amy两组肠道菌群差异较大,且在Δα-amy 包囊感染的小鼠中,肠道细菌(例如乳杆菌和拟杆菌、双歧杆菌、普雷沃菌、副普雷沃菌和Macellibacteroides)的相对丰度有所增加。菌群相关代谢物分析(Q200宏代谢组)发现,几种脂肪酸(壬二酸、辛二酸、α-亚麻酸ALA和柠檬酸)的浓度在Δα-amy组明显高于ME49组,其中ALA在Δα-amy组显著富集,此前有研究证实共生细菌乳酸杆菌和拟杆菌门可以产生肠菌源长链脂肪酸,具有很强的抗炎作用。
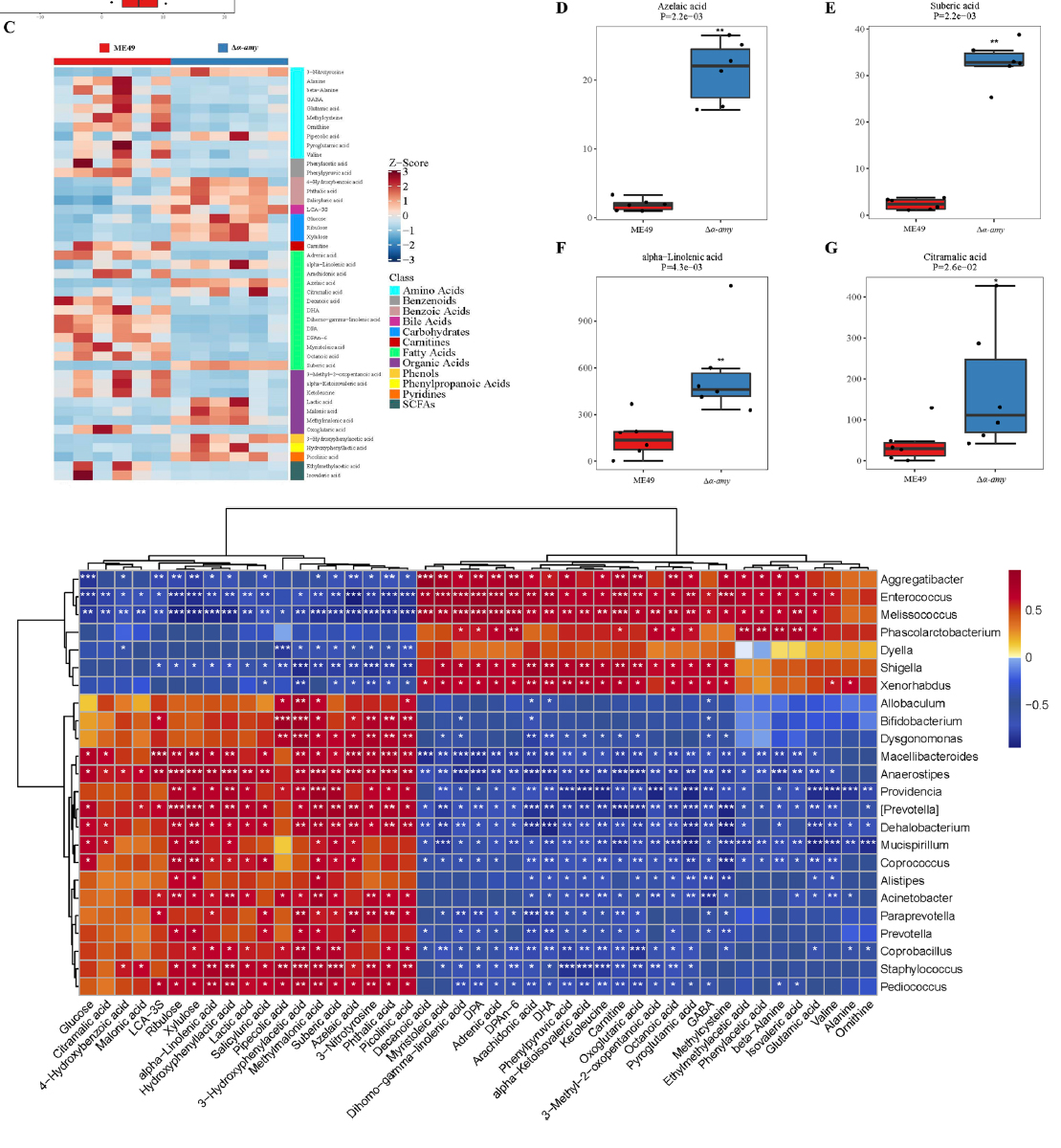
图4. 不同包囊感染小鼠粪便代谢组特征及相关性分析
4. 进一步通过口服ALA验证其作用机制发现,ALA可以通过改善宿主肠道微生物群的失调并通过MyD88/NF-κB途径抑制促炎细胞因子的产生来缓解弓形虫引起的肠道炎症严重程度。最后,来自ALA处理的供体小鼠的FMT重塑了弓形虫感染小鼠的肠道微生物群,减轻了弓形虫感染引起的肠道炎症反应。
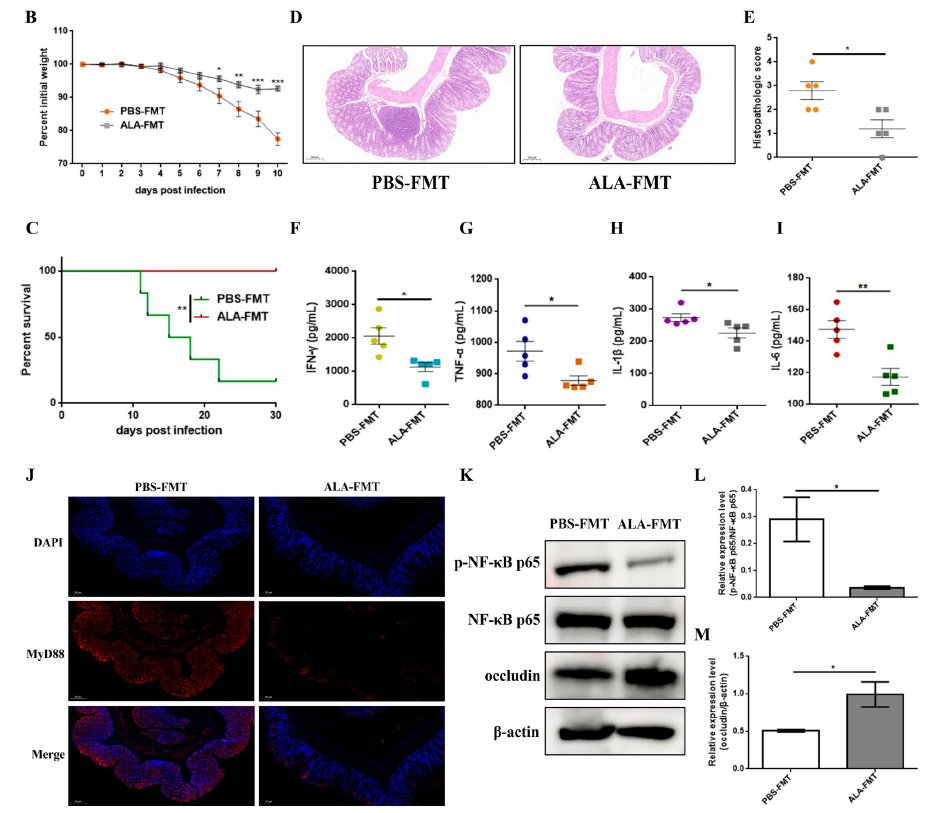
图5. ALA-FMT减轻弓形虫包囊感染引起的结肠炎
研究小结
本研究阐明了肠道微生物群和代谢物在弓形虫感染引起的结肠炎发展中的重要性,并揭示了ALA治疗弓形虫感染引起的致命肠道炎症的潜在效用,ALA通过MyD88/NF-κB通路改善肠道菌群失调,抑制炎症因子表达,减轻弓形虫诱导的肠道炎症。
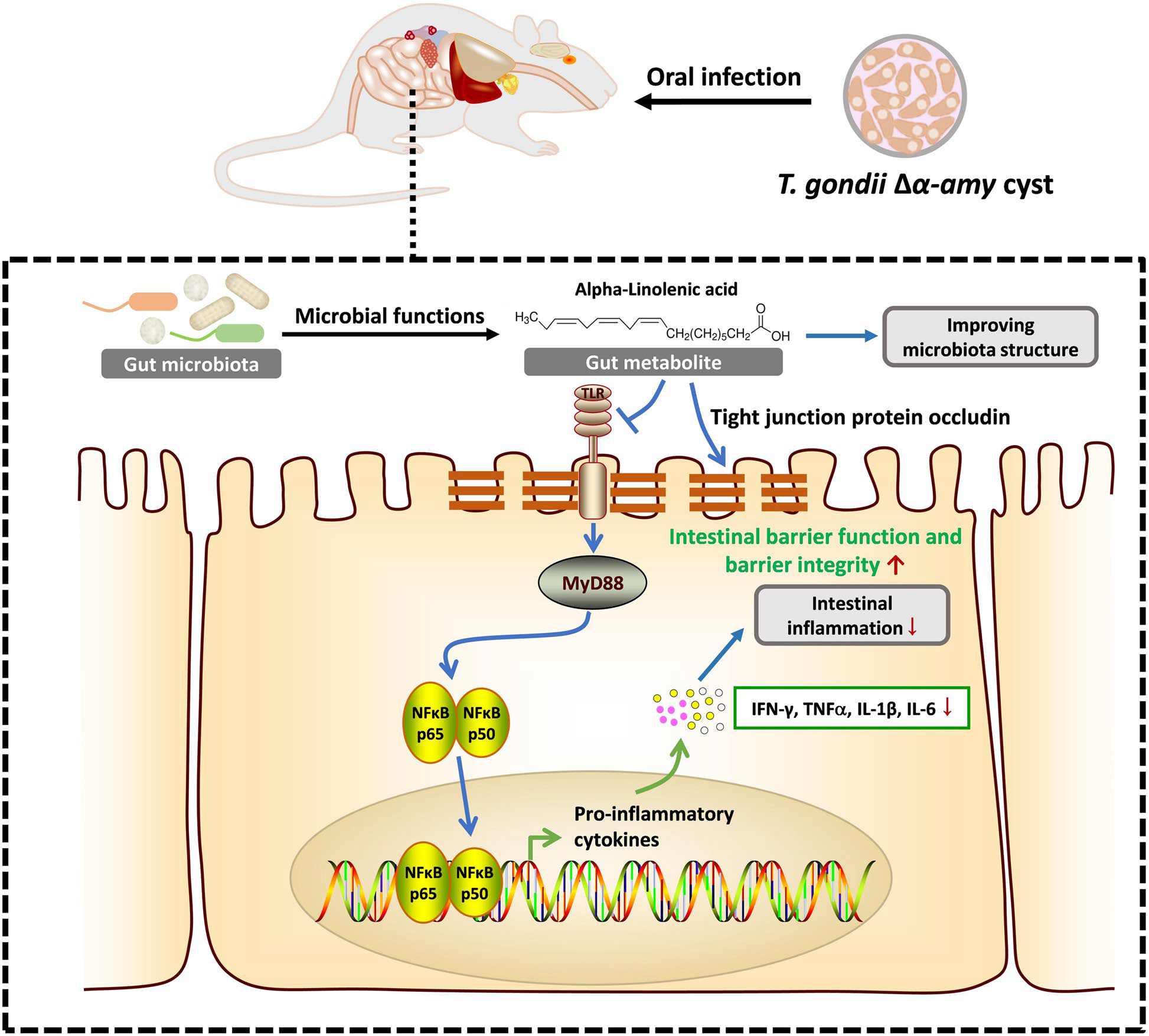
图6. 肠菌相关代谢物α-亚麻酸减轻弓形虫感染引起的肠道炎症
参考文献
Yang, J., Liu, S., Zhao, Q. et al. Gut microbiota-related metabolite alpha-linolenic acid mitigates intestinal inflammation induced by oral infection with Toxoplasma gondii. Microbiome. 2023
请扫描二维码阅读原文

绘谱帮你测
麦特绘谱拥有多套菌群相关特色产品,包括涵盖200+菌群宿主共代谢物的Q200宏代谢组,胆汁酸谱、色氨酸代谢物、短链脂肪酸等,以及16S和宏基因组测序。助力客户发表200+菌群代谢相关SCI文章,包括Nature, Cell Host & Microbe, Cell Metabolism, Gut, Microbiome等国际顶刊。
